审查
,卷:14(3)
Diels Alder反应- fmo和逐步自由基离子环加成途径
- *通信:
- Zargar ND,克什米尔大学化学系,斯利那加(190006),查谟和克什米尔,印度,电话:91 - 9906518251189;电子邮件: (电子邮件保护)
收到:2018年10月11日;接受:2018年10月26日;发表:2018年11月05日
引用:Zargar ND, Khan KZ。Diels Alder反应- fmo和逐步自由基离子环加成途径。化工学报。2018;14(3):131
摘要
碳(4+2)环加成二桤木反应一直是研究的课题。根据基态轨道的对称性,不同的二烯和亲二烯基团被用来进行这些正常的环加成反应。1,3-indandione也提供了diels alder反应的一个有趣的例子。亚胺(4+2)环加成反应被研究,其中亚胺或亚胺离子作为二嗜菌,为六元氮杂环的构建提供了强有力的工具。
研究了芳基乙烯基醚和相关底物的逐步自由基阳离子二元化反应莫达非尼在线畅销由氧化单电子转移(SET)过程触发的电催化进行,并通过独特的多条途径进行。
关键字
Cycloadditio;Diels alder反应;1、3-indandione;亚胺;激进的阳离子;亲二烯体;逐步地;氮杂环化合物
简介
一个正常的(4+2)环加成Diels Alder反应是共轭二烯和烯烃之间的同相轨道重叠和HOMO-LUMO结合。虽然在Diels Alder反应中使用了大量的二烯亲性试剂,但最近在热催化或酸催化条件下通过(4+2)环加成途径进行的异Diels Alder反应中,亚胺也被用作二烯亲性试剂。乙烯基酮与亚胺(4+2)环加成可得到产率极好的二氢吡啶酮[1].在类似的反应中,乙烯基等位烯也被发现在刘易斯酸存在下发生反应,产生高非对映选择性产物[2].
在更高级的研究工作中,通过氧化SET过程触发电催化,通过多种途径进行了逐步自由基阳离子Diels Alder反应。最近的自由基阳离子Diels - Alder反应的例子使用了苯乙烯,但范围不仅限于这种富电子的二嗜性物质。Bauld和Yoon观察到芳基乙烯醚、烯醇醚等价物和芳基乙烯基硫化物也可以作为有希望进行反应的二嗜烯试剂[3.-9].本文讨论了正周环(4+2)环加成与-à-vis自由基阳离子Diels Alder反应的多重反应机制。
一般讨论和机械路径
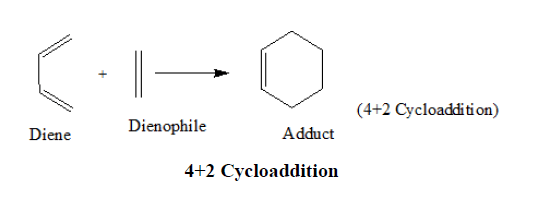
Diels - Alder反应是一个环加成反应,两个不饱和分子(二烯和二烯试剂)加在一起形成一个六元环[10].二烯是富电子亲核试剂,二烯是低电子亲电试剂。
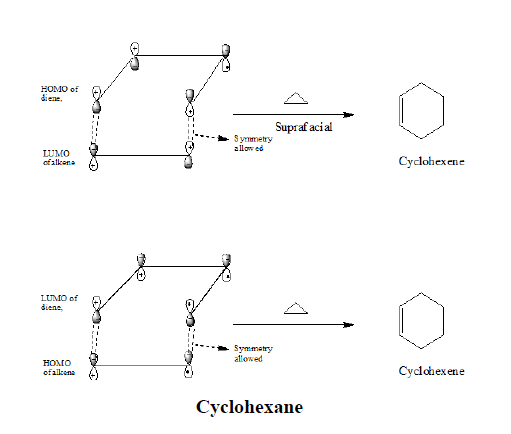
乙烯中接收这些电子的轨道是最低未占据分子轨道(LUMO)。丁二烯HOMO中的电子平稳地流入乙烯的LUMO中,从而产生一致的反应。自由基和离子中间体不涉及。
对(4+2)环加成反应的前沿轨道分析表明,形成两个新sigma键的同相轨道重叠需要面表面轨道重叠。这两种组合都是可能的如果我们用烯烃的HOMO和二烯的LUMO或者用烯烃的LUMO和二烯的HOMO。
两个基态轨道的对称性是这样的,终端叶瓣的键可以与表面几何发生。
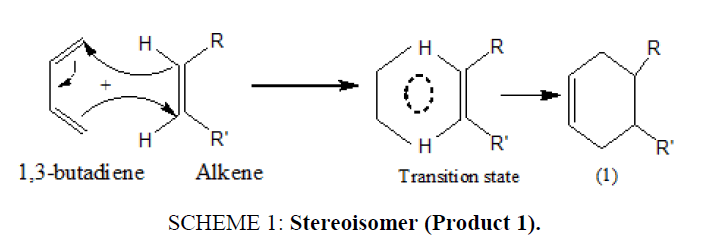
在这种环加成方法中,Diels Alder反应是立体定向的,并在热控制下进行。在反应过程中,起始二嗜物的立体化学保持不变,并且产生一个单一产物立体异构体(1),结果为(方案1).
计划1:立体异构体(产物1)。
通过没有中间产物的六中心过渡态,化学键同时断裂和生成。
同样地,如果我们与顺式二亲试剂(如甲基-顺-2-丁酸)进行环加成反应,则只生成顺式取代的环己烯产物(2)。
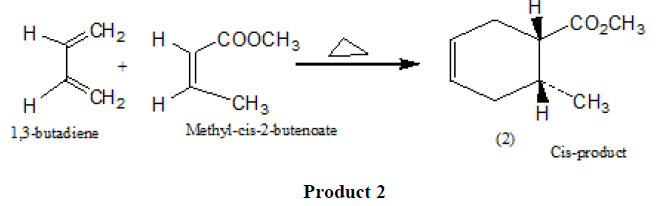
成千上万的Diels Alder反应的例子是由一个周环过程进行的。
二亲性试剂中的吸电子取代基如>C=O,-CHO,-COOR,-CN [11], no2 [12等等,促进反应。
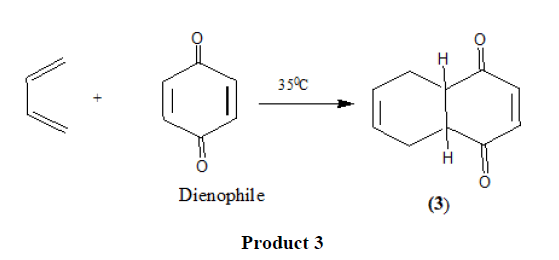
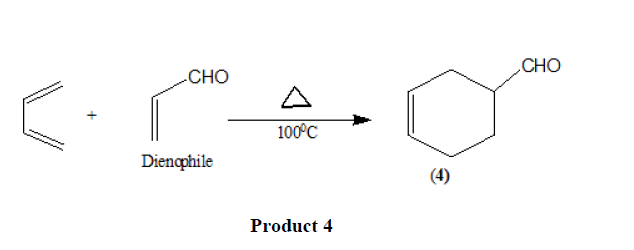
二烯中电子释放基团的存在也会加速反应。
三键化合物、等位基因和苯也可作为二嗜性物质[13].
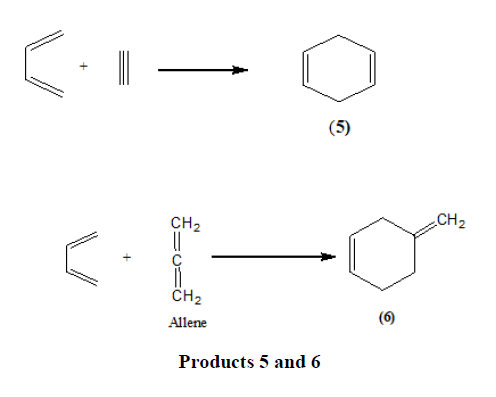
二烯也可能在芳烃体系中有一个双键,而在芳烃体系外有另一个双键。即。
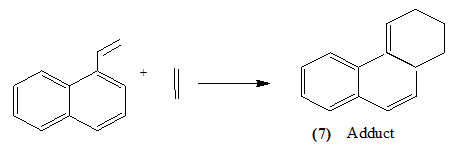
苯乙烯也以这种方式反应[14].
当环戊二烯和蒽与马来酸酐在不同条件下反应时,Endo产物(7a和7b)可产生高产量的Diels Alder反应[15-18].
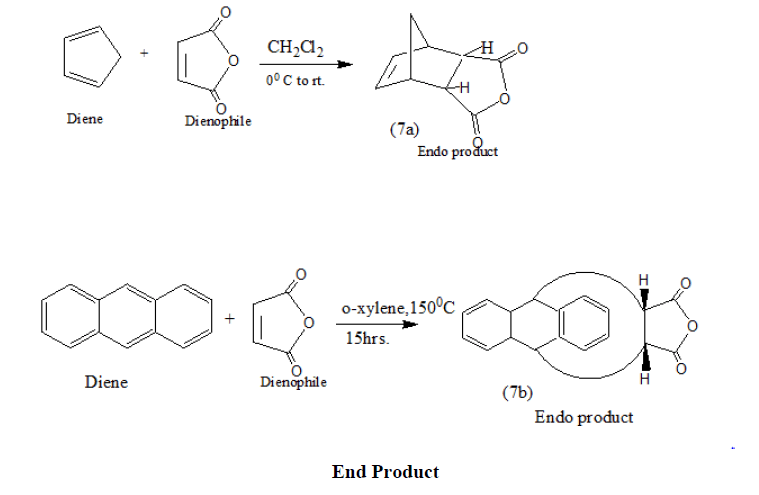
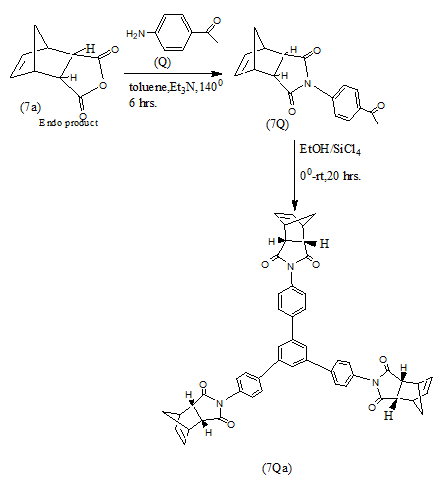
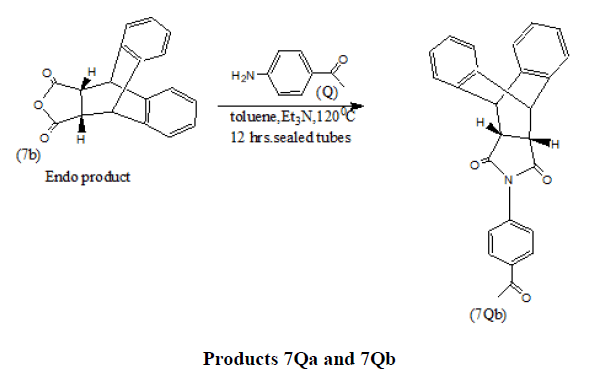
在最近的一项研究中,已从Diels Alder加合物(7a和7b)中合成了n个7Qa和7Qb型杂环,这些杂环加合物是使用适当的二烯和二嗜烯通过(4+2)环加成Diels Alder反应得到的[19].
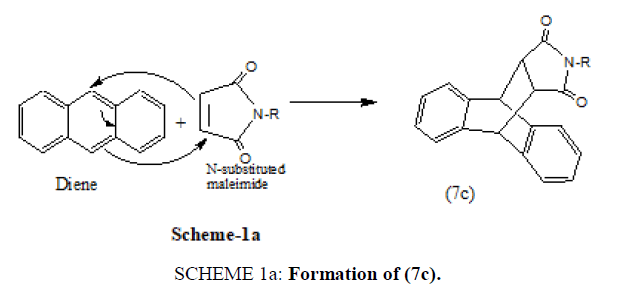
蒽还与n -取代马来酰亚胺反应生成Diels Alder加合物(7c) [20.].
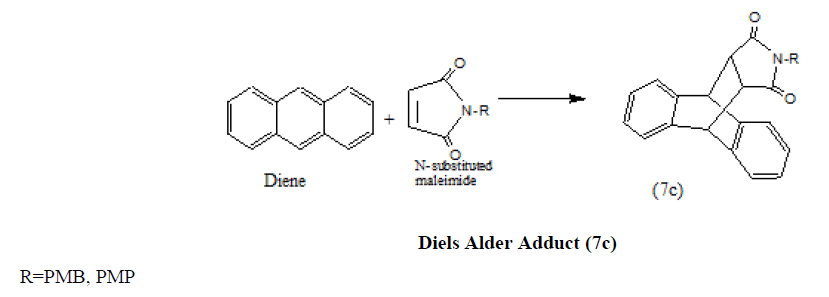
力学上(7c)的形成可以描述为(方案1).
计划1:形成(7c)。
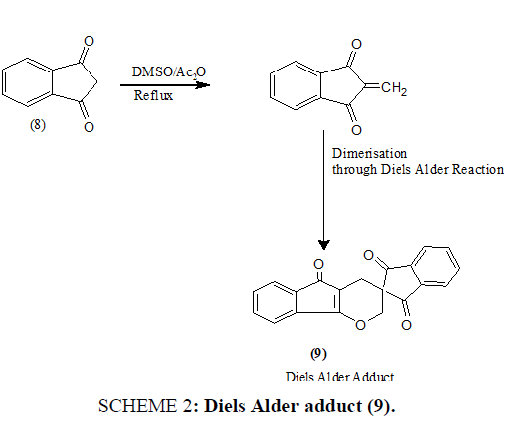
1,3-茚二酮(8)是1,3-二酮类化合物的重要成员,已发现在不同的底物和试剂下产生一系列具有生物和化学意义的化合物。当与DMSO/Ac相互作用时2O试剂在~1500°C,它提供一个Diels Alder加合物(9)方案2.
计划2:Diels Alder加和(9)。
在一个有趣的异- diels - Alder反应中,亚胺被用作涉及亚胺LUMO的二嗜性试剂。该反应可以是热催化或酸催化,并通过[4+2]环加成机制进行。
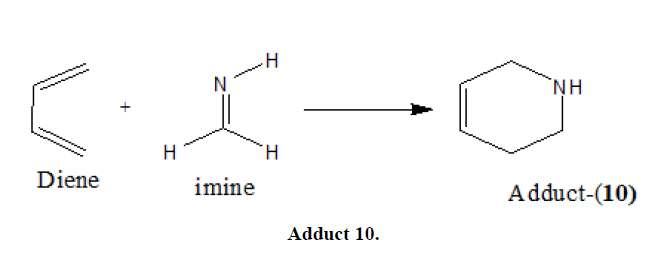
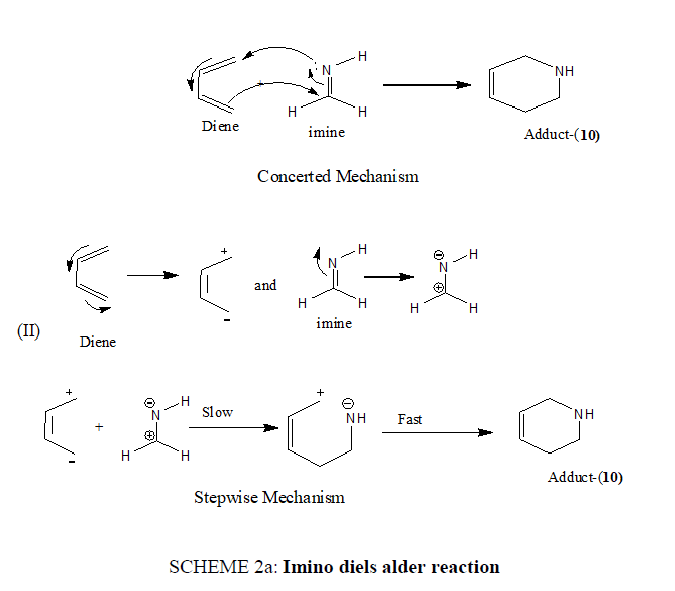
亚胺Diels - Alder反应可以通过协同机制或逐步过程发生(方案2).
计划2:Imino diels alder反应
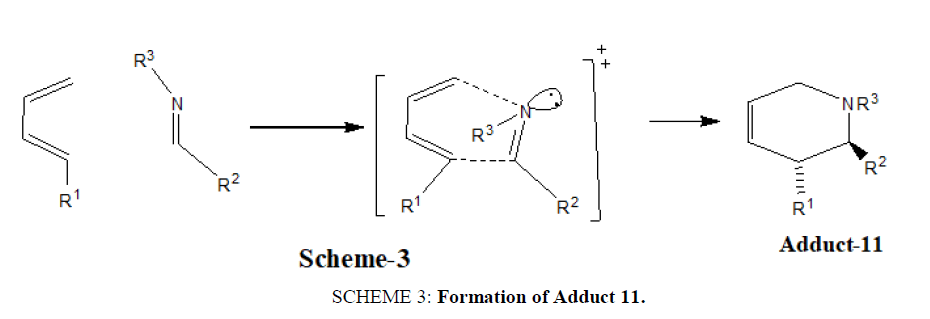
对于协调过程,最低能源过渡态使孤对处于外位。因此,在(E)亚胺中,孤对和较大的亚胺碳取代基是顺式的,倾向于产生外产物[21) (方案3).
计划3:加合物11的形成。
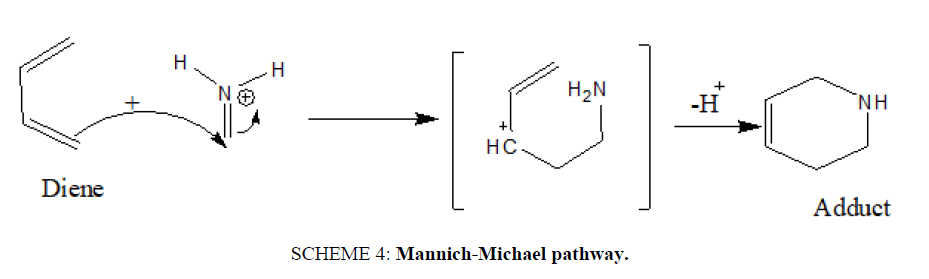
如果亚胺氮被质子化或配位到强刘易斯酸,则该机制转变为逐步的曼尼奇-迈克尔途径[22) (计划4).
计划4:Mannich-Michael途径。
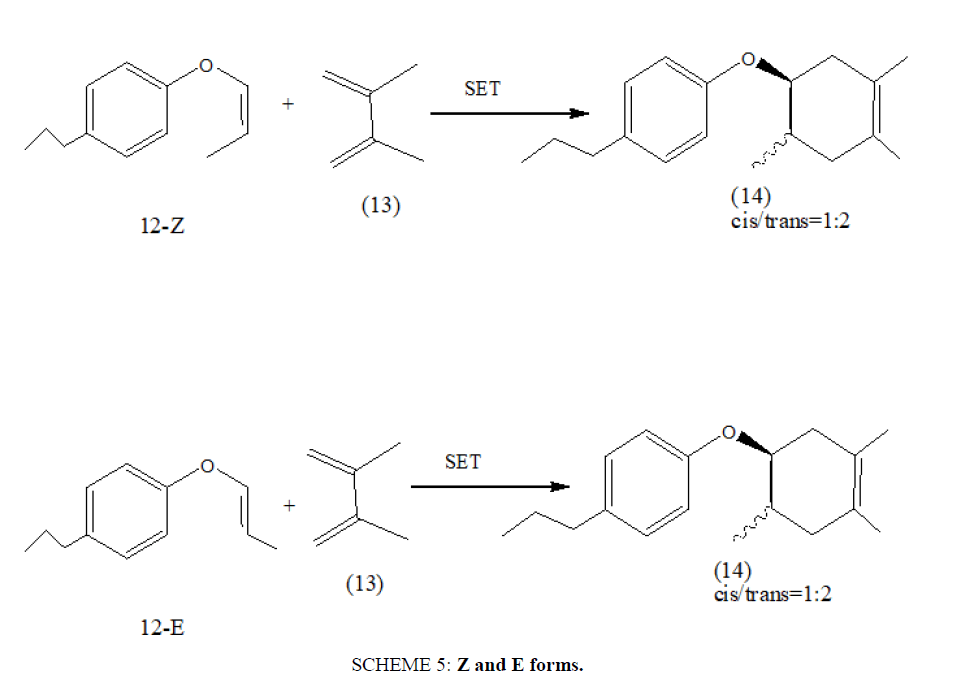
在最近的一项工作中,在单电子转移(SET)工艺下,芳基乙烯醚(12)与2,3-二甲基- 1,3-丁二烯(13)之间采用自由基阳离子Diels Alder反应,得到了收率很高的Diels Alder加合物(14)。加合物(14)被发现大约是顺式/反式=1:2的混合物,因此反应必须以循序渐进的方式进行。Z和E两种形式都能产生相同的合成产物[22) (计划5).
计划5:Z和E形式。
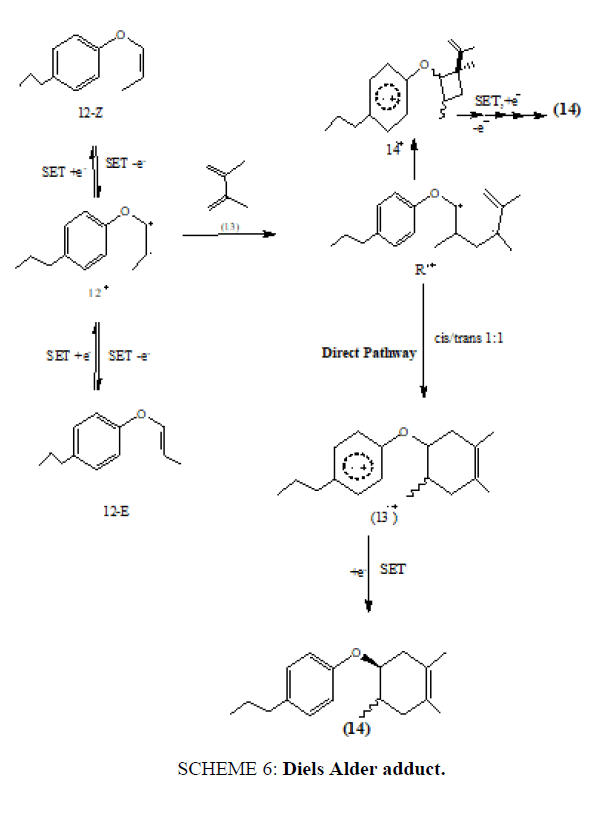
当芳基乙烯醚(12,E或Z)受到氧化SET条件的影响时,它提供了一个自由基阳离子(12+),然后被2,3-二甲基-1,3-丁二烯(13)捕获,得到丙烯酸基阳离子中间体(R.+)。这种无环自由基阳离子转化为具有六元环的芳香自由基阳离子(13+)或四元环(R.+)通过快速的分子内SET过程。这一机制表明,无环自由基阳离子中间体()的六元环闭环是一个逐步生成Diels Alder加合物(14)的过程(计划6) (表1).
计划6:Diels Alder加合。
| 反应名称 | 机制 | 加法类型 | 条件 |
|---|---|---|---|
| 正常Diels Alder反应 | 协同机制 | 4 + 2环加成作用 | 在热条件下进行 |
| 亚胺Diels Alder反应 | 协调和逐步机制 | 4 + 2环加成作用 | 热催化和酸催化 |
| 自由基Diels Alder反应 | 多种机制 | 4 + 2环加成作用 | 单电子转移(SET)过程 |
表1:不同反应条件下的Diels alder反应
合成应用
正常的Diels - Alder反应具有立体特异性,在合成中有广泛的应用。它已被用于合成许多天然产物,并通过研究加合物来确定反应物的构型。亚胺- Diels - Alder反应已被发现是合成许多天然产物的有力工具,通常以区域、非对映和对映选择的方式进行。给出了Diels - Alder反应的几个重要例子。
1.在camphine的合成中
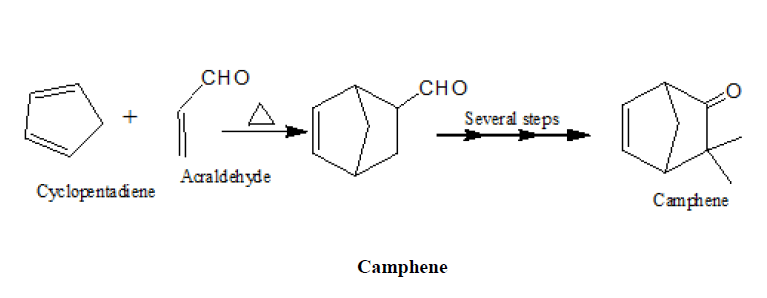
2.α-松蒎醇的合成
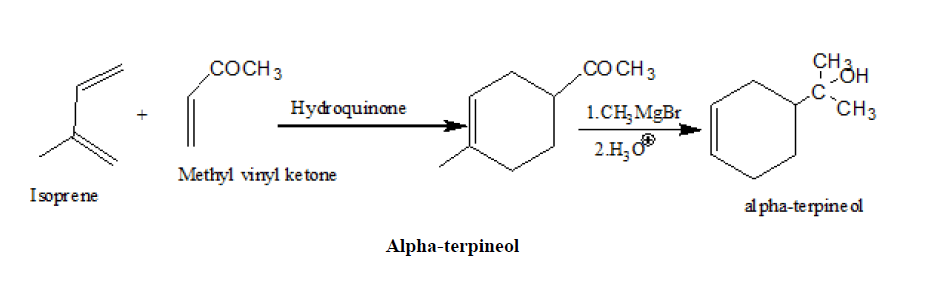
3.约翰逊合成欧雌酮
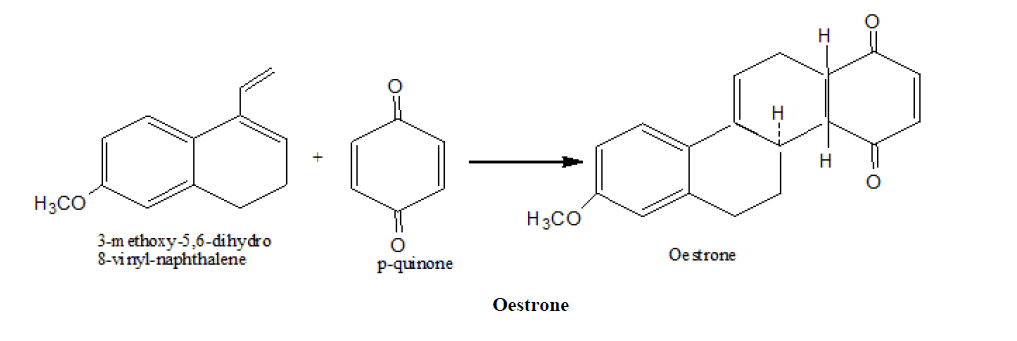
4.亚胺- Diels - Alder反应已被用于多种生物碱天然产物的合成
Danishefskys二烯用于构造一个六元环,在通往下叶氨酸的过程中[22].
结论
综上所述,我们的研究结果和文献调查表明,Diels - Alder反应不仅遵循协同机制,而且还遵循逐步机制途径。自由基离子Diels Alder反应具有高度的立体选择性,包括立体特异性的例子,并遵循氧化SET引发的环加成。在异- diels - Alder反应中,除了常见的二烯亲性物质外,亚胺也被用作二烯亲性物质。
鸣谢
我非常感谢我的导师KZ Khan教授,克什米尔大学化学系,在写这篇文章时给予了我鼓励和富有成效的建议。我也感谢印度斯利那加克什米尔大学的阿拉玛·伊克巴尔图书馆提供了本文的所有文献。
参考文献
- Bennett DM,冈本I, Danheiser RL。(三烷基硅基)乙烯酮的杂[4 + 2]环加成。不饱和戊内酯和内酰胺的合成。Org Lett 1999;1:641。
- Reg ' s D, Afonso MM, Rodr ' guez ML,等。通过Lewis酸催化乙烯基烯和亚胺反应合成八氢喹啉。化学工程学报,2003;
- 邵林,马仕柴,薛伟,等。可见光光催化自由基阳离子Diels-Alder环加成。化学学报。2011;33(3):357 - 357。
- 李文杰,李志强,李志强,等。阳离子自由基乙烯环丁烷重排。化学学报。1989;2:57-88。
- Pabon RA, Bellville DJ, Bauld NL。在阳离子自由基环加成中与Diels-Alder加成竞争形成选择性环丁烷加合物。化学学报,1984;26(3):344 - 344。
- Harirchian B, Bauld NL。有机合成中的阳离子自由基Diels-Alder环加成。(-)- β -selinene的形式全合成。化学学报。1989;11:1826-8。
- Aplin JT, Bauld NL。芳基乙烯硫化物作为亲电-电子转移机制的探针。化学Soc。PerkinTrans-2。1997; 5:853-5。
- Harirchian B, Bauld NL。《四面体杂志》199;28:927-30。
- 林淑娟,李士杰,葛伟,等。使用可切割氧化还原助剂的自由基阳离子环添加物。Org Lett. 2017;19:368-71。
- Brieger G, Bennett JN。分子内Diels-Alder反应。化学修订版1980;80:63-97。
- Butskus。基于丙烯腈的环化反应。俄罗斯化学Rev. 1962;31:28 -4。
- Novikov SS, Shvekhgeimer GA, Dudinskaya AA。二烯与硝基化合物合成。Russ Cheml Rev. 1960;29:79-94。
- Bastide和Henri-Rousseau, Willey,纽约,1978;67:447-552。
- 西加内克E.负取代乙炔。2苯乙烯的环加成反应。化学学报。1969;34:1923- 30。
- Kiriazis A, af Genn’s GB, Talman V,等。以蛋白激酶C. C1结构域为靶点的(3-氨基十氢- 1,4 -甲萘基-2-基)甲醇立体选择性合成。四面体。2011;67:8665-70。
- Kotha S, Todeti S, Aswar VR。通过环三聚化和闭环复分解序列设计和合成含有丙烯基团的c3对称分子。化学学报。2018;14:2537-44。
- 马什,亚当斯,H,巴克,MD,等。通过暂时去除内镜平面和立体烧蚀过还原对映选择性催化马来酰亚胺脱对称:(R)-吡咯仑的合成。2014; 6:3780-3。
- 张志强,张志强,等。有机合成用导电加热密封容器反应器的设计与性能验证。J Org Chem. 2016;81:11788-801。
- Whiting A, Windsor CM。是什么使中性亚胺二嗜生物发生热的、非催化的Diels-Alder反应?四面体。1998;54:6035-50。
- Waldmann, H。不对称异二元烯-桤木反应。合成。1994;6:535-51。
- 清水R,冈田Y,千叶k。多途径逐步自由基阳离子Diels-Alder反应。生物化学学报,2018;14(4):344 - 344。
- 韩国强,李志强,李志强,等。Securinega的全合成生物碱(+)- 14,15 -二氢securinine,(-)-去甲securinine和叶嘌呤。化学工程学报,2000;