原文
,数量:2 (1)
原发性肝癌的治疗的进步
- *通信:
- 阿什拉夫克,生物学系、基础科学研究所大不里士大学大不里士,伊朗,电话:98-411-33393924,电子邮件: (电子邮件保护)
收到:2016年6月24日;接受:2016年6月29日;发表:2016年7月7日
引用:阿什拉夫·g·DUF538基于实时rt - pcr检测基因表达在Drought-Challenged Celosia。生物化学杂志2016;2 (1):101
文摘
原发性肝癌症(PLC)是常见的恶性肿瘤之一。发病率高,预后不良,PLC已成为的一个主要疾病是严重危害人类生命和健康。近年来,研究工作一直在总结原发性肝癌的治疗的地位,已经取得了很大的进步,特别是重大进展的早期诊断、手术治疗和综合治疗肝脏癌症做出改善的生活质量的患者。尽管许多方法可以用来提高生活质量,仍有问题需要深入研究。的治疗研乐动体育在线究进展的综述肝脏癌症本文所做的可能为此类疾病的进一步治疗提供帮助。
关键字
Celosia;干旱胁迫;DUF538;基因表达;实时聚合酶链反应
介绍
DUF538蛋白质总科由几种植物蛋白的未知函数。DUF538是唯一重要的,可辨认的保守域已经报道了这种蛋白质总科,迄今为止。蛋白质这个总科的成员已经在大范围的单子叶植物的分布和双子叶植物物种(1,2]。他们估计分子量约为19 kDa 21周围kDa编码170个氨基酸。最近,三维花瓣——就像。的结构拟南芥DUF538蛋白质已经决定了核磁共振和释放到通用的蛋白质数据库(PDB ID: D1ydua1)。它已被证明拥有蛋白质结构由β-strands主导。
几百DUF538推导氨基酸序列的通用数据库中沉淀为假想的蛋白质。但是,没有这种蛋白质超家族的成员迄今为止发现的藻类和蓝细菌(2]。DUF538域包含蛋白质主要是确定使用基因组注释工具也被克隆为诱导基因从植物的挑战与营养缺乏等各种环境压力(基因库,BFT415717),冠瘿病(基因库,BG131101)和混合(基因库,AW040635)从细胞内番茄,和轻微的干旱杨树(基因库,CU232042)Celosia植物(基因库,AJ535713)没有实时分析和比较其表达水平(3]。的基础上高磷酸化潜力,DUF538蛋白质预测中发挥重要的监管角色不同stress-challenged植物(4]。我们的报告显示,体内应用融合形式DUF538蛋白质利用植物组织研磨材料激活植物的氧化还原系统细胞(1]。
在最近的一项研究中,DUF538蛋白质都被认为会影响细菌生长速率通过绑定到外层膜上的脂多糖分子的细菌膜一样杀菌渗透率增加蛋白在哺乳动物先天免疫系统5]。之后,通过使用生物信息学工具,DUF538三级结构预测是类似于esterase-type水解酶或酶分解脂肪的羧基esterease B型,acyl-peptide水解酶,entrochelin esterease,和过氧化物酶病长链酰coa水解酶是最好的匹配(6]。
保持所有这些信息视图,DUF538成员可能被建议作为一种常见的植物系统与压力相关的策略。在目前的研究工作,作为我们的研究的一部分,增加我们的知识有关的可能角色DUF538蛋白质总科植物系统,我们试图调查DUF538的表达谱基因表达的叶组织Celosia cristata植物与干旱胁迫的挑战。
材料和方法
化学物质
试剂盒试剂(猫。不。RN7713C;RNX™;总RNA CinnaGen)是用于隔离,信使核糖核酸纯化试剂盒提供的工具包是,美国(猫。No.70022)。互补脱氧核糖核酸合成AcessQuickTM rt - pcr系统从Promega购买(猫。不。A1701)。SYBR绿色染料用于实时检测基因表达来自生物Rad公司。Fermentas DNA提取工具包(猫。不。K0513)是用于净化的聚合酶链反应从琼脂糖凝胶产品。质粒载体pGEM-T容易(猫。不。A1360;Promega)被用于聚合酶链反应克隆产品。本研究工作中使用所有的其他化学物质的分子生物学的成绩。
植物材料
的种子Celosia cristata股票被从我们的实验室。测试植物可以生长在普通实验室条件下每天晚上和湿度。为了收集叶子材料,测试植物浇水直到六叶期之后的水被保留直到植物明显沿条。干旱压力状况持续了4周。实验材料的收集,从叶组织之前和之后压力治疗。
总RNA隔离和mRNA净化
总细胞RNA分别孤立从测试材料使用试剂盒试剂,分别。大约0.2 g的每一个材料是细粉使用液体N2和2毫升的试剂盒试剂在室温下是添加到同质化(RT)。200μl氯仿被添加到混合,混合了15秒,孵化冰上5分钟和离心机13000 rpm,持续15分钟。上层阶段被转移到另一个管和RNA与同等体积的异丙醇沉淀。的颗粒在1毫升的75%乙醇洗,干在RT和溶解在30μl RNase-free水。RNA的完整性测试non-denaturing 1%琼脂糖凝胶使用此种运行缓冲。保利(+)核糖核酸纯化使用益生元从总RNA dT-columns根据协议提供的工具包。纯化mRNA的完整性也分析了电泳使用1% non-denaturing琼脂糖凝胶。RNA在起始原料的数量在接下来的实验测量spectrophotometrically [7]。
引物设计和互补脱氧核糖核酸的合成
特定的引物用于放大设计基于已经报道DUF538记录序列(3]。在线网络Primer3软件设计的引物序列。
为了分析DUF538基因的表达模式,使用一步法rt - pcr反应分别执行AcessQuick™rt - pcr系统。约0.5μg每个信使rna样本混合25μl大师混合(2 x)和1μl记者底漆。混合物被调整到最后一卷50μl使用nuclease-free水。反应混合物在45°C 45分钟和孵化之前聚合酶链反应骑自行车。聚合酶链反应进行了在95°C pre-denaturation阶段后3分钟在25个周期。使用底漆的核苷酸序列的设置和细节聚合酶链反应步骤进行我们的以前的工作1),在表1。
| PremierSequences | |
| 离开温家宝:5 ' C G C C T T C T T T G G C C 3 ' | |
| 对温家宝:5 ' C T C T C C C G C T C G一百一十一3 ' | |
| PCR扩增步骤 | |
| 变性 | 95年\ C / 1分钟 |
| 退火 | 55 \ C / 1分钟 |
| 扩展 | 72 \ C / 1.5分钟 |
| 最后扩展 | 72 \ C / 10分钟 |
表1:总理集&聚合酶链反应放大的步骤。
在下一步中,放大产品从琼脂糖凝胶中提取,克隆在pGEM-T容易克隆载体(7]。克隆的片段进行测序的Microsynth DNA测序中心瑞士。
实时逆转录PCR分析表达式
DUF538记录在测试样本的表达水平进行了分析通过实时rt - pcr使用智商SYBR绿色supermix Miniopticon实时(生物Rad)聚合酶链反应检测系统(生物Rad)。实验中执行三个复制和数据的平均值。所有的表达数据归一化通过调节肌动蛋白基因的表达水平在测试样品和相对使用2折计算表达式-ΔΔCt值(8]。
孤立的片段的序列分析
放大的互补的核苷酸序列进行了分析计算在爆炸(基本局部比对搜索工具)http://www.ncbi.nlm.blast.com/和CLASTALW序列比对软件http://www.genome.jp/和Expasy蛋白质组学工具http://www.expasy.org/tools/。
结果与讨论
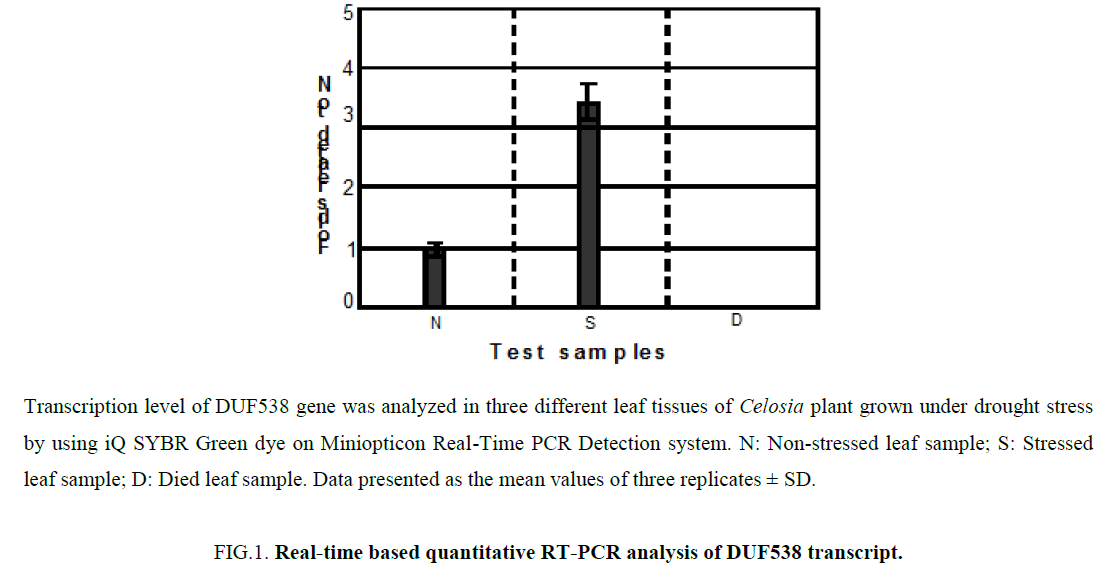
在前面的工作中,我们发现了一个干旱压力诱导DUF538基因的叶子Celosia cristata植物(3]。rt - pcr分析终端产品1%琼脂糖凝胶上显示的表达DUF538成绩单一直有叶材料的检测和强调样本。只有死叶组织未能收集到的样本显示DUF538的证据基因表达在琼脂糖凝胶。这里,我们扩展表达式研究实时分析干旱的挑战Celosia工厂。从叶组织' DUF538表达基因,之前报道的引物对的CelosiaDUF538使用(3]。存在和DUF538转录水平的表达被实时rt - pcr检测方法使用测试样本收集的叶组织在三个时间点包括有,压力和死亡。图1显示了相对折叠的表达和量化DUF538基因的表达水平变化在三个不同叶样品。所有数据规范化和相关L0(有叶样品视为控制)使用2-ΔΔCt值(8]。喜欢以前的结果通过琼脂糖凝胶,分析2-ΔΔ可靠地显示Ct值CelosiaDUF538基因表达在强调和有叶测试样品除了干叶材料。结果表明,DUF538不同的表达水平有压力和样本。结果表明:DUF538基因的表达水平是相当高的压力挑战组织(图1)。相比,有组织,有大约3.2 - -3.6折”强调增加叶样品。DUF538的表达水平被发现没有被实时表达分析在琼脂糖凝胶干燥叶样品。结果表明,DUF538基因的表达水平增加强调的叶子Celosia工厂。
为了分析强调和有放大产品的序列,克隆和测序。核苷酸序列比较分析结果显示,强调和有组织的放大cDNA 100%相同(核苷酸序列数据不是)。比较他们的推导氨基酸序列CLASTALW软件显示放大的互补的氨基酸序列与之前报道的100%和50% DUF538互补脱氧核糖核酸Celosia工厂和美国东部时间杨树(3)(图2)。
DUF538基因的表达基本先前报道rt - pcr方法从不同的植物生长在充满压力的环境条件下,如营养缺乏(基因库,BFT415717),冠瘿病(基因库,BG131101)和混合等(AW040635基因库,轻度干旱杨树(基因库,CU232042)Celosia植物(基因库,AJ535713) [3]。所有这些数据表达我们的知识没有实时分析和比较基因表达的水平。目前的实时数据与DUF538有关基因表达表明DUF538蛋白成员高度诱导在干旱条件下,可能等drought-stressed植物的潜在作用Celosia。它已经明白,干旱的产品压力诱导基因分为功能和调节蛋白。各种环境的调控蛋白调节压力信号转导通路。他们通常知道控制其他stress-inducible基因的表达在植物系统[9- - - - - -11]。其中包括各种转录因子、蛋白激酶蛋白磷酸酶,酶参与磷脂代谢和其他信号分子如钙调蛋白结合蛋白(12,13]。根据本构以及应激基因表达DUF538蛋白质的成员Celosia植物和考虑其他stress-challenged植物下的表达式,DUF538蛋白质总科似乎假定候选人共同与压力相关的蛋白质可能共同调节因子可能参与了各种各样的植物压力响应。
的基因表达概要文件的植物暴露于干旱压力之前分析的微阵列技术和其他分子和基因组学方法特别是在拟南芥和大米植物。伴侣蛋白分子,晚胚胎发生丰富的蛋白质,渗透,osmolyte生物合成的酶,抗冻蛋白,mRNA-binding蛋白质,水通道蛋白,糖和氨基酸转运蛋白,解毒酶,氧化蛋白质和各种水解酶蛋白酶等著名的干旱胁迫相关元素(14,15]。DUF538之间的相似性得分高家庭成员和水解酶酶(5)可能是一个有力的线索DUF538域包含的干旱胁迫相关的生物活性蛋白质在植物。这个提议在未来需要进一步澄清。
当前实时数据可能表明DUF538基因活性可能的干旱压力在植物的防御反应系统。我们调查的分布DUF538成员通过互联网直接同源聚类分析表明,DUF538总科广泛分布于双子叶植物和单子叶植物植物(图3)。基部被子植物门,蕨类植物和苔藓也发现有这种蛋白质。但是,动物,绿藻,红藻类、真菌、抗议和原核生物没有发现含有DUF538蛋白质。DUF538分布格局的真核生物光合作用意味着这种蛋白质的功能性质总科可能是守恒的,它在光合生物可能发挥重要作用。另一方面,最近提名DUF538蛋白质家庭作为哺乳动物的潜在结构和功能同系物杀菌蛋白在植物提供基础研究的强有力的抗应激功能的蛋白质家庭也或者他们的同系物在哺乳动物中,(5]。
作为一个初步报告,我们希望我们的结果将提供一个新的研究门研究详细bio-physiological DUF538基因产物在植物或动物的角色系统环境压力刺激。
确认
这项研究的作者是感谢研究所基本科学,大不里士大学伊朗支持这项工作。
引用
- 阿什拉夫•g .逆境应答的不同的表达DUF538域包含蛋白质及其morpho-biochemical后果。植物j . 2011; 30 (5): 351 - 8。
- 高桥年代,Yoshikawa M, Kamada, et al .藜的photoconvertible水溶性蛋白质chlorophyll-binding DUF538成员总科,分布在陆生植物。J植物杂志。2013;170 (17):1549 - 52。
- 阿什拉夫G, Kohnehrouz SB.IdentificationDUF538cDNA克隆物从Celosia cristata表示相应的序列和强调。57 RussJPlant杂志。2010;(2):247 - 52。
- Nakagami H, Sugiyama N, Mochida K, et al。大规模比较phosphoproteomics标识守恒的磷酸化网站在植物。植物杂志。2010;153 (3):1161 - 74。
- 阿什拉夫G, Kohnehrouz某人ProtJ.2013; 32:163。
- 阿什拉夫G。预测三级结构之间的同源性杀菌/通透性增加蛋白先天免疫系统和水解酶的酶。IntJBiosci。2014;5 (2):1 - 6。
- 奥苏贝尔调频,布伦特R,金斯敦,摩尔DD, Seiolman詹,史密斯是当前分子生物学技术等。。纽约:约翰·威利& Sons;1991年。
- Livak KJ, Schmittgen TD。分析的相对基因表达数据使用实时定量聚合酶链反应和2−ΔΔCT方法。方法。2001;25 (4):402 - 8。
- 马,Maruyama M,安倍H, et al .监测表达谱大米基因在寒冷、干旱、和盐碱地压力和脱落酸的应用程序使用芯片技术和RNA gel-blot分析。植物杂志。2003,133 (4):1755 - 67。
- Shinozaki K,山口SK,尹浩然,塞其监管网络基因表达在干旱和寒冷压力响应。CurrOpinPlant杂志。2003;6 (5):410 - 7。
- Shinozaki K,山口SK。基因网络参与干旱压力响应和宽容。JExpBot。58 2007;(2):221 - 7。
- 山口SK, Shinozaki k cis-acting监管组织元素渗透,cold-stress-responsive推动者。植物科学的趋势。2005;10 (2):88 - 94。
- 巴特尔D, Sunkars r .干旱和盐耐受性植物。CritRevPlant Sci, 2005; 24 (1): 23-58。
- 塞其M, Narusaka M,安倍H, et al .监测1300个拟南芥基因的表达模式在干旱和寒冷强调通过使用一个完整的芯片。植物细胞。2001;13 (1):61 - 72。
- Schimid M,戴维森TS,老母鸡,等。基因表达拟南芥发展的地图。NatGenet。2005年,37 (5):501 - 6。