简短的沟通
,卷:14(3)
丙氧肟形式易合成E和Z异构体
- *通信:
- 上海金江苏大学药学院,镇江212013电话:+ 86-511-85038451;电子邮件: (电子邮件保护)
收到:2018年9月9日;接受:2018年9月25日;发表:2018年10月05日
引用:何大伟,何奥林,金国帆,等。丙氧肟形式易合成E和Z异构体。化工学报,2018;14(3):129
关键字
Celosia;干旱胁迫;DUF538;基因表达;实时聚合酶链反应
简介
采用不同的合成途径合成了甲基-(E-Z)-2-(2-(2,5-二甲基-4-(E-Z)-1-(丙氧亚氨基乙基)苯氧基)甲基)-3-甲氧基丙烯酸酯,分别称为A和B。通过巧妙的合成方法,分别采用A和B方法获得了高选择性肟形式的E-和Z-异构体,收率分别为96%和94%。
E-Z异构体常出现在化工、材料、制药等领域,但分离E和Z异构体较为困难。在本研究中,肟衍生物的E-Z异构体可以通过两种不同的途径选择性地合成。
实验
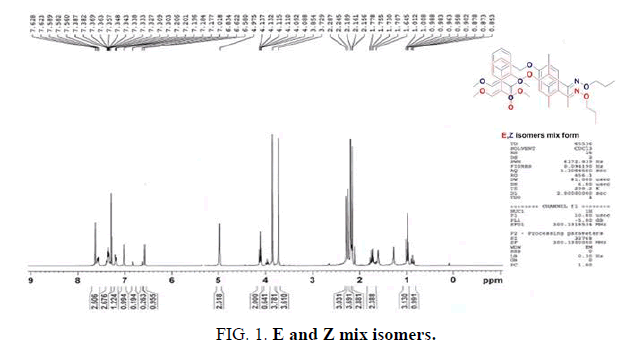
所有操作都在干燥的氮气下进行大气使用标准Schlenk技术。乙腈(ACN)和甲醇购自阿拉丁纯化学公司。反应在默克F-254预涂薄层塑料片上进行监测,使用己烷作为流动相。所有产率均为柱后产物的孤立产率色谱法使用硅胶(200-230目)。所有玻璃器皿、注射器、磁力搅拌棒和针都在对流烤箱中干燥一夜。在操作的布鲁克300光谱仪上记录了1H-NMR谱,并测量了相对于锁定溶剂(99.9% CDCl)的内部残留峰的化学位移3.),然后引用Si(CH3.)4(0.00 ppm)。元素分析使用Carlo Erba Instruments CHNS-O EA1108分析仪(图1-3.).
结果与讨论
本文报道了甲基-2-(2-(溴甲基)苯基)-3-甲氧基丙烯酸酯部分,如2,6-二甲基苯酚、羟胺和1-溴丙烷,它们是在碳-氧或碳-氮化学键结合上合成的。采用A和B方法得到了这些化合物具有较高选择性的异构体结构。
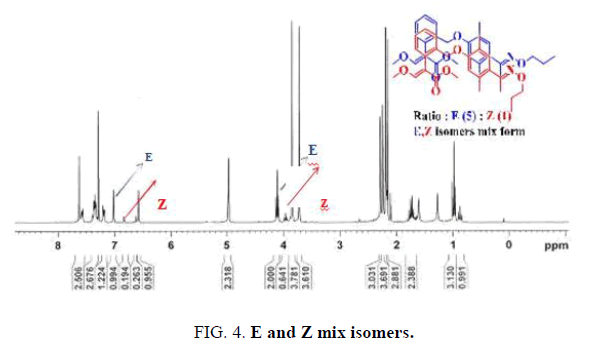
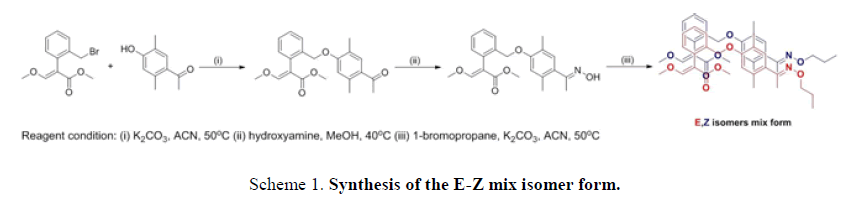
甲基-2-(2-(2,5-二甲基-4-(E)-1-(丙氧亚氨基乙基)苯氧基)甲基)苯基)-3-甲氧基丙烯酸酯的一般制备过程包括一系列反应,如亲电取代、Friedel-Crafts反应和基本条件下的胺化反应。方案1而且图4) [1-6]。
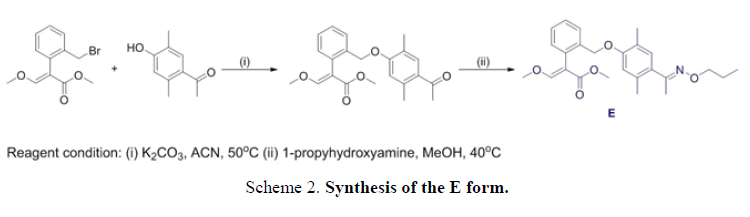
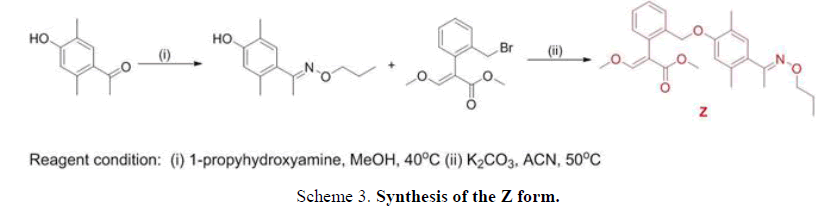
用常规方法得到混合异构体,根据1H-NMR谱,E-Z异构体比为5:1,如图所示图4.下面报告使用不同的方法解决上述问题的详细步骤(方案2而且方案3).
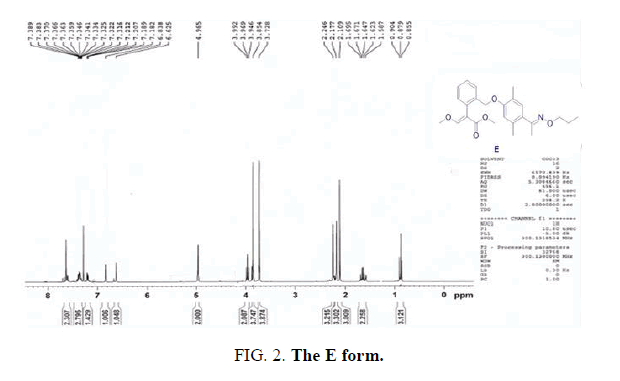
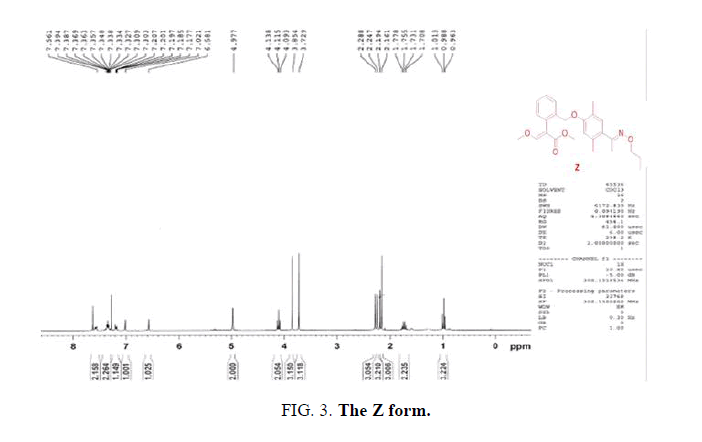
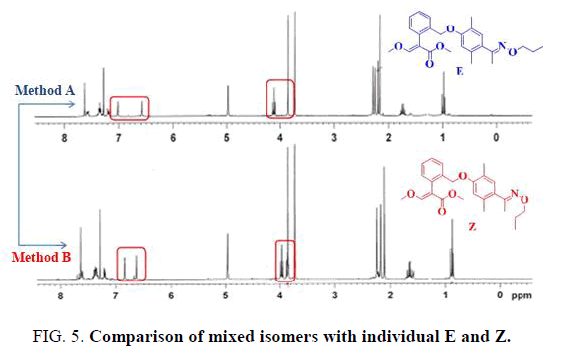
通过巧妙的设计路线分别合成了E和Z目标化合物。1 h - nmr光谱学揭示的值在两个单峰之间的芳香环在7.0-6.5 PPM范围内,一个三峰和单峰在4.4-3.8 PPM范围内。在中等产率(E 96%和Z 94%)下,得到了不同程度的E和Z异构体图5所示。
综上所述,考虑到目标化合物的结构性质、可行性和分析性质,我们采用简单的合成路线合成了肟衍生物的E和Z异构体。从改进的合成路线中获得的知识将有助于最终产品的选择和评估。
方法
合成methyl-2 - (2 - (2, 5-dimethyl-4 - (E) 1 - (propoxyimino)乙基)苯氧基)甲基)苯基)3-methoxyacrylate(单体E)。一个解决方案的甲基2 - (2 - ((4-acetyl-2 5-dimethylphenoxy)甲基)苯基)3-methoxyacrylate(1.6克,4.3更易)和O-propylhydroxylamine(0.4克,5.2更易)在15毫升的甲醇在室温下搅拌30分钟,然后加热40°C下3 h。原油产品集中,和残渣被闪光柱纯化色谱法(乙酸乙酯/己烷1:6)得到单体E:产率:1.8 g(96%)。1 hnmr (CD3Cl),δ,ppm: 7.61(年代,1 h), 7.59 - -7.54 (m, 1 h), 7.39 - -7.33 (m, 2 h), 7.20 - -7.18 (m, 1 h), 7.02(年代,1 h), 6.58(年代,1 h), 4.97 (s, 2小时),4.13 - -4.09 (t, J = 6.9赫兹,2 h), 3.85(年代,3 h), 3.72(年代,3 h), 2.28(年代,3 h), 2.24(年代,3 h), 2.19(年代,3 h), 1.77 - -1.70 (m, 2 h), 1.01 - -0.96 (t, J = 7.5赫兹,2 h)。Found, %: C70.35;H 7.40;3.43 N。C25H31没有5.计算,%:C 70.33;H 7.38;3.41 N。
方法B
甲基-2-(2-(2,5-二甲基-4-(Z)-1-(丙氧亚氨基)乙基)苯氧基)甲基)苯基-3-甲氧基丙烯酸酯(单体Z)甲基-2-(2-(溴甲基)苯基)-3-甲氧基丙烯酸酯(2.3 g, 8.1 mmol)和碳酸钾(1.3 g, 8.9 mmol)在20 mL乙腈中室温搅拌30分钟。随后,在室温下加入1-(4-羟基-2,5-二甲基苯基)比-1- 1氧基氧肟(3.6 g, 8.5 mmol),然后在50℃下加热5 h,粗产物浓缩,用闪蒸柱纯化渣油色谱法(乙酸乙酯/己烷1:6)得到单体Z:产率:2.8 g(94%)。1 hnmr (CD3Cl),δ,ppm: 7.68 - -7.59 (m, 1 h), 7.62(年代,1 h), 7.38 - -7.31 (m, 2 h), 7.21 - -7.18 (m, 1 h), 6.83(年代,1 h), 6.62(年代,1 h), 4.96 (s, 2小时),3.99 - -3.94 (t, J = 6.9赫兹,2 h), 3.85(年代,3 h), 3.72(年代,3 h), 2.24(年代,3 h), 2.17(年代,3 h), 2.10(年代,3 h), 1.69 - -1.58 (m, 2 h), 0.90 - -0.85 (t, J = 7.5赫兹,2 h)。Found, %: C70.36;H 7.42;3.47 N。C25H31没有5.计算,%:C 70.31;H 7.36;3.42 N。
突出了
1.难以分离E和Z异构体
2.不同的路径,A和B
3.通过巧妙的合成方法
4.它们具有高度选择性的肟形式
5.个人E和Z
图形抽象
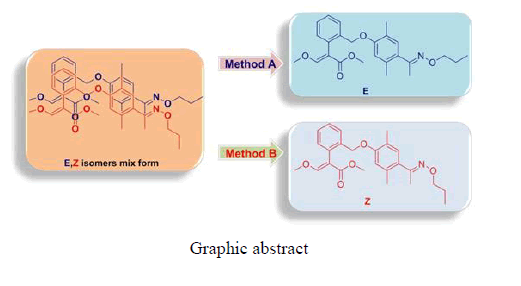
本文报道了甲基-(E- z)-2-(2-(2,5-二甲基-4-(E- z)-1-(丙氧亚氨基乙基)苯氧基)甲基)苯基)-3-甲氧基丙烯酸酯的E-和z -异构体的合成,研究了它们的高选择性肟型。
鸣谢
本研究得到江苏大学科研基金项目(No. 5501290005)的资助。
参考文献
- Fuse S, Otake Y, Mifune Y,等。单流Arndt?法快速制备A -芳基羧酸Eistert合成。Aust J Chem. 2015;68:1657-61。
- Cvijetic IN, Tan ø M, Juranic IO,等。5-芳基- 1h -吡唑-3-羧酸作为人碳酸酐酶IX和XII的选择性抑制剂。生物医学化学。2015;23:4649-59。
- 张晓明,张晓明,张晓明,等。手性乙酸锌配合物催化亚胺对映选择性硅氢化反应。化学学报。2015;
- Sathyanarayana P, Ravi O, Muktapuram PR,等。铜催化氧辅助C (CNOH)?C(alkyl) bond cleavage: a facile conversion of aryl/aralkyl/vinyl ketones to aromatic acids. Org Biomol Chem. 2015;13:9681-5.
- 王海燕,Mueller DS, Sachwani RM,等。邻乙烯基肟醚的[3,3]有序重排形成碳-碳键并合成吡咯。Org Lett. 2010;12:2290-3。
- 李志强,李志强,李志强,等。《生物化学》2004;2:415-20。